Kết hợp thuốc đích và hóa trị điều trị đột biến KRAS G12C trong ung thư phổi
15:47 - 08/05/2025
Tổng quan chiến lược phối hợp thuốc đích sotorasib, adagrasib và hóa trị trong điều trị ung thư phổi không tế bào nhỏ (UTPKTBN) mang đột biến KRAS G12C: dữ liệu lâm sàng, cơ chế và triển vọng.
Khối u giảm càng nhiều, sống càng lâu: Giá trị tiên lượng trong điều trị ung thư phổi đột biến EGFR
Giảm khối u càng sâu, sống càng lâu: Đột phá trong điều trị ung thư phổi EGFR bằng thuốc nhắm trúng đích
Thuốc đích EGFR trong điều trị ung thư phổi giai đoạn 4: Thời gian lui bệnh và ý nghĩa lâm sàng
Hiệu quả thuốc đích Osimertinib trong điều trị di căn gan ung thư phổi đột biến EGFR+ giai đoạn 4
Kết hợp thuốc đích và hóa trị trong điều trị ung thư phổi không tế bào nhỏ mang đột biến KRAS G12C
I. Mở đầu
Ung thư phổi không tế bào nhỏ (UTPKTBN, tiếng Anh: NSCLC – Non-Small Cell Lung Cancer) là nguyên nhân hàng đầu gây tử vong do ung thư trên toàn cầu. Trong số các đột biến gen liên quan đến UTPKTBN, KRAS G12C được xem là một đột biến phổ biến và khó điều trị. Đột biến này chiếm khoảng 13% các trường hợp UTPKTBN và là mục tiêu điều trị nổi bật gần đây nhờ sự ra đời của các thuốc ức chế KRAS G12C như sotorasib và adagrasib.
Tuy nhiên, một thách thức quan trọng là hiệu quả đơn trị của các thuốc đích KRAS G12C thường bị giới hạn bởi hiện tượng kháng thuốc sớm và không đồng nhất sinh học của khối u. Do đó, các chiến lược kết hợp với hóa trị đang được nghiên cứu nhằm mục tiêu kéo dài thời gian kiểm soát bệnh (PFS), tăng tỷ lệ đáp ứng (ORR), và giảm nguy cơ kháng thuốc. Bài viết này tập trung phân tích các bằng chứng tiền lâm sàng, lâm sàng và hướng nghiên cứu tương lai liên quan đến phối hợp thuốc đích KRAS G12C và hóa trị.
II. Cơ sở sinh học của KRAS G12C và vai trò phối hợp hóa trị
1. KRAS G12C – Mục tiêu đột biến mới đầy tiềm năng
KRAS là một GTPase điều hòa các tín hiệu tăng sinh tế bào thông qua các con đường MAPK (Mitogen-Activated Protein Kinase) và PI3K/AKT/mTOR. Đột biến G12C khiến KRAS bị "kẹt" trong trạng thái hoạt hóa (gắn GTP), dẫn đến kích hoạt liên tục các tín hiệu sinh ung thư. Các thuốc như sotorasib và adagrasib hoạt động bằng cách gắn kết cộng hóa trị vào cysteine tại vị trí đột biến, giữ KRAS ở trạng thái bất hoạt (GDP-bound).
2. Lý do phối hợp với hóa trị
Phối hợp hóa trị và thuốc đích KRAS G12C có thể tăng hiệu quả điều trị nhờ các cơ chế sau:
Tiêu diệt tế bào không phụ thuộc KRAS: hóa trị có phổ tác động rộng, tiêu diệt cả các tế bào không mang đột biến KRAS hoặc mang đột biến kháng mắc phải. Điều này hỗ trợ thuốc đích hoạt động hiệu quả hơn trên quần thể còn lại.
Giảm tải lượng khối u: hóa trị có thể nhanh chóng làm giảm số lượng tế bào ác tính, giảm áp lực chọn lọc đột biến kháng thuốc, từ đó giúp thuốc đích kiểm soát bệnh bền vững hơn.
Tăng tính thấm của thuốc đích: hóa trị có thể phá vỡ cấu trúc mô đệm và hàng rào mạch máu trong vi môi trường u, giúp thuốc đích thâm nhập sâu hơn vào mô khối u.
Tăng cường miễn dịch kháng u: một số hóa chất (như pemetrexed, platinum) có thể làm tăng trình diện kháng nguyên và kích hoạt đáp ứng miễn dịch, tạo điều kiện thuận lợi để phối hợp thêm liệu pháp miễn dịch hoặc thuốc đích có tác dụng gián tiếp lên miễn dịch.
Tác động hiệp lực trên nhiều con đường tín hiệu: hóa trị và thuốc đích cùng tác động vào các cơ chế khác nhau trong chu trình sống của tế bào ung thư, giúp giảm nguy cơ kháng chéo và tăng hiệu quả tổng thể.
Hóa trị giúp phá vỡ môi trường miễn dịch u ức chế và gây chết tế bào theo cơ chế không phụ thuộc KRAS.
Giảm tải lượng tế bào ung thư, từ đó tăng hiệu quả của thuốc đích.
Phối hợp làm chậm quá trình phát triển kháng thuốc qua con đường bù như EGFR, MET, HER2.
III. Dữ liệu lâm sàng nổi bật về phối hợp thuốc đích và hóa trị
1. Sotorasib kết hợp hóa trị
a. Thử nghiệm CodeBreaK 300
Thiết kế: Nghiên cứu pha III so sánh sotorasib kết hợp với docetaxel so với docetaxel đơn trị ở bệnh nhân UTPKTBN mang KRAS G12C đã điều trị toàn thân trước đó.
Mục tiêu chính: PFS theo đánh giá của chuyên gia độc lập (BICR).
Kết quả sơ bộ (2024):
PFS trung vị: 5.5 tháng (sotorasib + docetaxel) vs 4.2 tháng (docetaxel đơn)
Tỷ lệ đáp ứng khách quan (ORR): 20.7% vs 9.0%
Tỷ lệ kiểm soát bệnh (DCR): 72.8% vs 60.3%
Tác dụng phụ độ 3–4: xảy ra ở 33.3% nhóm phối hợp, chủ yếu là giảm bạch cầu, tiêu chảy, tăng men gan
Ý nghĩa lâm sàng: Phối hợp sotorasib + docetaxel cải thiện rõ rệt hiệu quả điều trị bước hai, đặc biệt phù hợp bệnh nhân có tiến triển sau liệu pháp miễn dịch hoặc hóa trị chuẩn trước đó.
b. Thử nghiệm SCARLET (NCT04933695)
Thiết kế: Thử nghiệm pha 1b/2 đánh giá tính an toàn và hiệu quả của sotorasib kết hợp hóa trị (carboplatin + pemetrexed) ở bệnh nhân UTPKTBN có đột biến KRAS G12C chưa từng điều trị toàn thân.
Cỡ mẫu: 36 bệnh nhân.
Liều dùng: Sotorasib 960 mg/ngày kết hợp hóa trị mỗi 3 tuần trong 4 chu kỳ, sau đó duy trì bằng sotorasib ± pemetrexed.
Kết quả bước đầu:
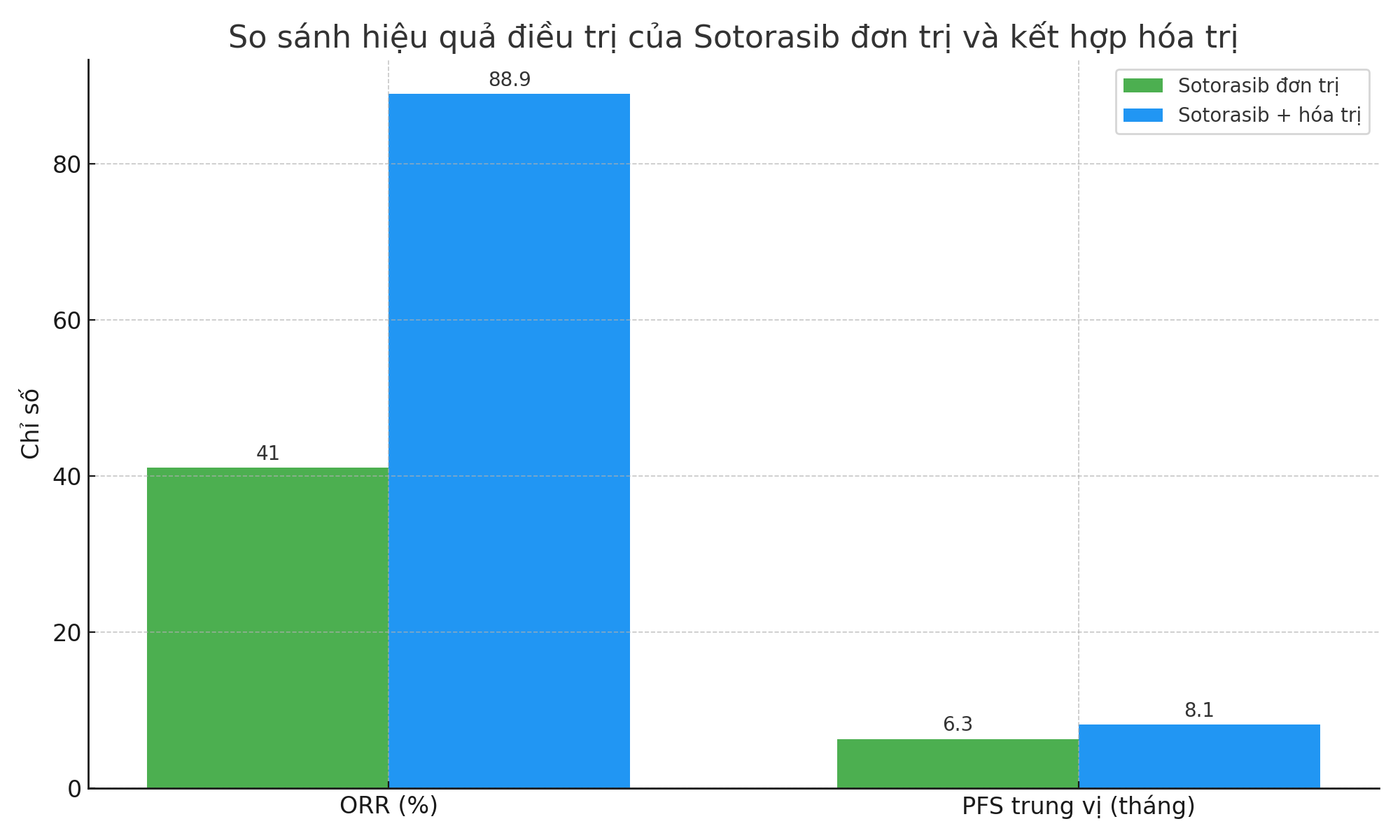
Tỷ lệ đáp ứng khách quan (ORR): 88.9%
Tỷ lệ kiểm soát bệnh (DCR): 94.4%
PFS trung vị: 5.7 tháng (tính tại thời điểm theo dõi 9.5 tháng)
Tác dụng phụ thường gặp:
Độ 3–4: giảm bạch cầu trung tính (11.1%), buồn nôn (8.3%), mệt mỏi (5.6%)
Không ghi nhận độc tính mới vượt trội so với đơn trị
Ý nghĩa lâm sàng: kết hợp cho thấy hiệu quả cao, dung nạp tốt, hứa hẹn trở thành lựa chọn điều trị hàng đầu (first-line) cho bệnh nhân KRAS G12C nếu được xác nhận qua các thử nghiệm pha III rộng hơn.
Thiết kế: Sotorasib kết hợp carboplatin + pemetrexed ở bệnh nhân KRAS G12C chưa từng điều trị.
Kết quả sơ bộ:
ORR: 88.9%
PFS trung vị: 5.7 tháng
Tác dụng phụ độ 3–4 xảy ra ở 40% bệnh nhân, chủ yếu là giảm bạch cầu và buồn nôn.
Đánh giá: Hiệu quả cao, có thể là liệu pháp lựa chọn bước đầu (first-line) nếu xác nhận qua pha III.
2. Adagrasib kết hợp hóa trị
a. Thử nghiệm KRYSTAL-12
Thiết kế: Nghiên cứu pha III so sánh adagrasib đơn trị với docetaxel ở bệnh nhân UTPKTBN mang KRAS G12C đã điều trị toàn thân trước đó.
Mục tiêu chính: PFS theo đánh giá RECIST 1.1.
Kết quả đang chờ công bố. Tuy nhiên, dữ liệu từ nghiên cứu KRYSTAL-1 cho thấy hiệu quả vượt trội khi kết hợp hóa trị.
b. Thử nghiệm KRYSTAL-1 (mở rộng)
Adagrasib phối hợp carboplatin + pemetrexed hoặc docetaxel ở bệnh nhân bước 2 trở đi.
ORR: dao động từ 54–65%
PFS: khoảng 6–7 tháng
Ưu điểm: đáp ứng nhanh, kiểm soát triệu chứng tốt, phù hợp nhóm không dung nạp liệu pháp miễn dịch hoặc có gánh nặng khối u cao.
c. Tác dụng phụ thường gặp
Tăng men gan, buồn nôn, tiêu chảy, giảm bạch cầu trung tính độ 3.
Tỷ lệ ngưng điều trị do độc tính dưới 10%, cho thấy dung nạp tốt.
d. Ý nghĩa lâm sàng
Dữ liệu hỗ trợ adagrasib có thể được sử dụng kết hợp hóa trị như một lựa chọn chiến lược điều trị sau thất bại miễn dịch hoặc hóa trị đơn độc, đặc biệt ở nhóm bệnh nhân có yếu tố tiên lượng xấu.
e. Dữ liệu KRYSTAL-1
Adagrasib kết hợp carboplatin + pemetrexed hoặc docetaxel trong điều trị bước 2.
ORR dao động từ 54–65% tùy phác đồ.
PFS: 6–7 tháng
Ưu điểm: ổn định khối u sớm, kiểm soát tốt triệu chứng.
IV. Cơ chế phối hợp và lợi ích sinh học
1. Tác động hiệp lực sinh học
Hóa trị tiêu diệt các tế bào không phụ thuộc KRAS → tạo môi trường thuận lợi cho thuốc đích hoạt động.
Giảm chọn lọc các dòng tế bào mang đột biến kháng mắc phải (ví dụ: Y96D, G13D).
2. Tăng tính miễn dịch của khối u
Hóa trị làm tăng trình diện kháng nguyên u (tumor antigen presentation).
Kết hợp với thuốc đích → làm tăng hiệu quả nếu thêm liệu pháp miễn dịch sau đó.
3. Kiểm soát vi mô u (microenvironment)
Hóa trị phá vỡ hàng rào mạch máu, tăng thấm thuốc đích vào khối u.
Điều hòa miễn dịch và giảm các tế bào T ức chế (Treg).
V. So sánh đơn trị và phối hợp hóa trị
| Phác đồ | ORR (%) | PFS trung vị (tháng) | Ghi chú |
|---|---|---|---|
| Sotorasib đơn | ~41 | 6.3 | CodeBreaK 100 |
| Sotorasib + hóa trị | 65–88.9 | 5.7–8.1 | SCARLET & NCT04625647 |
| Adagrasib đơn | 43 | 6.5 | KRYSTAL-1 |
| Adagrasib + hóa trị | 54–65 | 6–7 | Đang theo dõi |
VI. Thách thức và lưu ý lâm sàng
1. Độc tính chồng lấp
Cần theo dõi độc tính huyết học, tiêu hóa khi phối hợp.
Giảm liều hóa trị trong một số trường hợp để tối ưu cân bằng hiệu quả/độc tính.
2. Thời điểm tối ưu để phối hợp
Liệu có nên dùng sớm ngay từ đầu (first-line)? Hay đợi đến khi kháng đơn trị?
Cần thêm dữ liệu từ thử nghiệm pha III để khẳng định.
3. Chỉ định cho đối tượng cụ thể
Phối hợp có thể đặc biệt hiệu quả ở bệnh nhân có PD-L1 thấp, không có di căn não, hoặc không dung nạp miễn dịch.
VII. Tương lai và hướng nghiên cứu
Các thử nghiệm đang tiến hành: SCARLET, KRYSTAL-12, CodeBreaK 300, NCT04929245.
Sử dụng biomarker (ví dụ: TP53, STK11, KEAP1) để xác định nhóm có lợi từ phối hợp.
Kết hợp “bộ ba” hóa trị + thuốc đích + miễn dịch cũng đang được nghiên cứu (triplet therapy).
VIII. Kết luận
Phối hợp thuốc ức chế KRAS G12C và hóa trị liệu là một hướng đi tiềm năng nhằm vượt qua giới hạn của liệu pháp đơn trị. Dữ liệu hiện có cho thấy hiệu quả cao hơn, kiểm soát tốt hơn và thời gian đáp ứng kéo dài hơn so với dùng riêng lẻ. Tuy nhiên, việc triển khai rộng rãi cần dựa trên dữ liệu từ các nghiên cứu pha III và được cá thể hóa dựa trên đặc điểm sinh học của bệnh nhân.
Cần tư vấn chuyên sâu về các thuốc điều trị ung thư phổi:
- ThS – BS Trần Khôi
- Bệnh viện Phổi Hà Nội – 44 Thanh Nhàn, Hai Bà Trưng
- Zalo: 0983 812 084 – Hotline: 0913 058 294
- Facebook: Bác sĩ Trần Khôi
- Kênh YouTube: Thạc sĩ Bác sĩ Trần Khôi – Chữa bệnh ung thư phổi




