Hiệu quả thuốc đích Osimertinib trong điều trị di căn gan ung thư phổi đột biến EGFR+ giai đoạn 4
09:25 - 22/05/2025
Phân tích chuyên sâu hiệu quả Osimertinib đối với di căn gan trong ung thư phổi EGFR+, so sánh đơn trị và kết hợp hóa trị, kèm dữ liệu nghiên cứu mới nhất.
Khối u giảm càng nhiều, sống càng lâu: Giá trị tiên lượng trong điều trị ung thư phổi đột biến EGFR
Giảm khối u càng sâu, sống càng lâu: Đột phá trong điều trị ung thư phổi EGFR bằng thuốc nhắm trúng đích
Thuốc đích EGFR trong điều trị ung thư phổi giai đoạn 4: Thời gian lui bệnh và ý nghĩa lâm sàng
Hiệu Quả Thời Gian Sống Thêm Không Tiến Triển (PFS) Của Thuốc Đích EGFR Trong Ung Thư Phổi Giai Đoạn 4
Giới thiệu
Ung thư phổi không tế bào nhỏ (UTPKTBN) chiếm khoảng 85% tổng số ca ung thư phổi. Trong số này, khoảng 10–20% bệnh nhân có di căn gan tại thời điểm chẩn đoán hoặc trong quá trình điều trị. Di căn gan là một trong những yếu tố tiên lượng xấu, liên quan đến khả năng kháng thuốc, diễn tiến nhanh và thời gian sống rút ngắn.
Osimertinib, thuốc ức chế tyrosine kinase EGFR (EGFR-TKI) thế hệ 3, đã được chứng minh hiệu quả vượt trội trong điều trị bệnh nhân UTPKTBN có đột biến EGFR, đặc biệt là exon19del và L858R. Tuy nhiên, hiệu quả của Osimertinib tại nhóm bệnh nhân có di căn gan vẫn đang được nghiên cứu và là thách thức lâm sàng đáng kể.
Hiệu quả của Osimertinib đối với di căn gan
2.1 Dữ liệu từ nghiên cứu "Clinical efficacy of osimertinib in EGFR-mutant NSCLC patients with liver metastases"
- Thời gian sống không tiến triển (PFS):
- Bệnh nhân có di căn gan: 7,4 tháng
- Bệnh nhân không có di căn gan: 19,7 tháng
- Thời gian sống toàn bộ (OS):
- Di căn gan: 12,1 tháng
- Không di căn gan: chưa đạt (Not reached)
- Tỷ lệ đáp ứng khách quan (ORR): giảm rõ rệt ở nhóm có di căn gan, không khác biệt nhiều so với các EGFR-TKI thế hệ 1 và 2.
2.2 Giải thích cơ chế giảm hiệu quả
Di căn gan ảnh hưởng đến hiệu quả của Osimertinib thông qua nhiều cơ chế sinh học và miễn dịch:
- Vi môi trường viêm và miễn dịch ức chế đặc hiệu của gan: Gan là cơ quan có tính dung nạp miễn dịch cao. Sự hiện diện của nhiều tế bào miễn dịch điều hòa (regulatory T cells), đại thực bào M2 và các phân tử ức chế miễn dịch như IL-10, TGF-β góp phần tạo điều kiện thuận lợi cho tế bào ung thư "ẩn náu" khỏi hệ thống miễn dịch. Điều này làm giảm hoạt tính gây độc của thuốc đích.
- Nồng độ cao VEGF và IGF-1: Cả VEGF (vascular endothelial growth factor) và IGF-1 (insulin-like growth factor 1) đều có vai trò trong tăng sinh mạch máu và sinh tồn tế bào ung thư. Những yếu tố này không chỉ thúc đẩy sự phát triển của khối u gan mà còn làm giảm hiệu quả của EGFR-TKI bằng cách kích hoạt các con đường tín hiệu thay thế (bypass signaling).
- Kháng thuốc do chuyển hóa gan: Gan là cơ quan chính trong chuyển hóa thuốc. Enzym CYP3A4 và các transporters như ABCB1 có thể làm giảm nồng độ Osimertinib nội mô tại vị trí di căn, làm giảm hiệu quả tác dụng dược lý.
- Tính chất phân tử học của tế bào di căn gan: Một số nghiên cứu đã chỉ ra rằng tế bào ung thư khi di căn đến gan có biểu hiện gen và sự hoạt hóa con đường tín hiệu khác biệt (MET, AXL, PI3K/AKT/mTOR), khiến chúng ít nhạy cảm hơn với ức chế EGFR đơn thuần.
Cải thiện hiệu quả bằng chiến lược phối hợp
3.1 Dữ liệu từ nghiên cứu "Efficacy of EGFR-TKIs monotherapy versus TKI plus chemotherapy in advanced NSCLC with liver metastases"
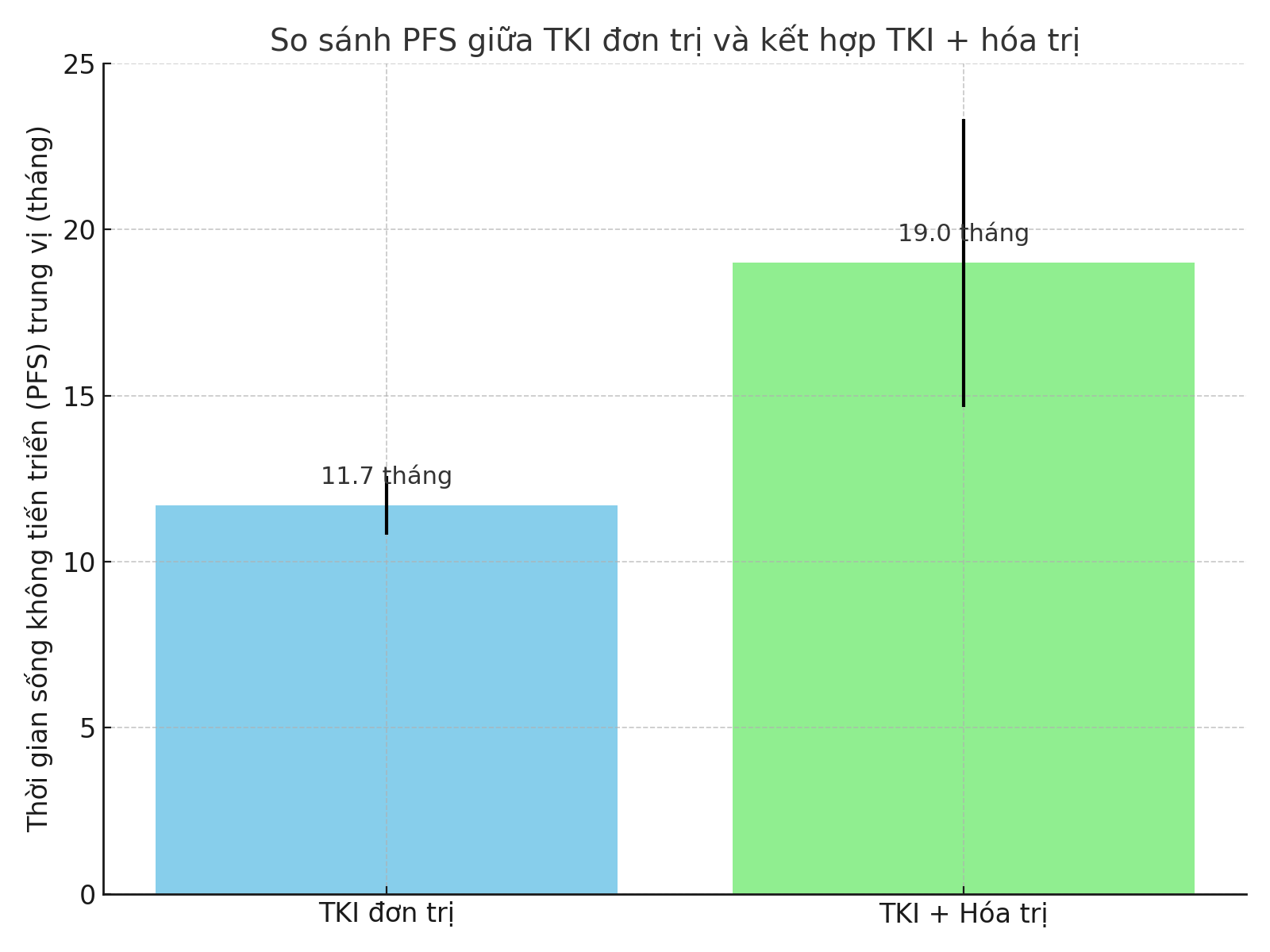
Nghiên cứu so sánh hiệu quả giữa nhóm điều trị bằng EGFR-TKI đơn thuần và nhóm kết hợp EGFR-TKI với hóa trị (pemetrexed + platinum):
- PFS trung vị:
- Nhóm kết hợp: 19,0 tháng (95% CI: 14,67–23,33)
- Nhóm đơn trị: 11,7 tháng (95% CI: 10,81–12,59) → p < 0,001
- OS trung vị:
- Nhóm kết hợp: chưa đạt
- Nhóm đơn trị: 38,5 tháng → p = 0,586
- Tỷ lệ đáp ứng (ORR):
- Nhóm kết hợp: 78,0%
- Nhóm đơn trị: 64,2% → p = 0,108
- Tỷ lệ kiểm soát bệnh (DCR):
- Kết hợp: 98,0% | Đơn trị: 97,0%
3.2 Theo từng đột biến EGFR:
- Exon 19 deletion:
- PFS nhóm kết hợp: 20,93 tháng | Đơn trị: 11,77 tháng → p = 0,004
- L858R:
- PFS nhóm kết hợp: 18,07 tháng | Đơn trị: 11,17 tháng → p = 0,021
3.3 Phân tích theo mức độ đột biến EGFR:
- Mức độ đột biến cao:
- PFS kết hợp: 19,0 tháng | Đơn trị: 10,93 tháng → p = 0,008
- Mức độ đột biến thấp:
- PFS kết hợp: 11,83 tháng | Đơn trị: 10,57 tháng → p = 0,545
3.4 Tác dụng phụ:
- Nhóm kết hợp có tăng các biến cố huyết học:
- Giảm bạch cầu (44% vs 7,5%), giảm tiểu cầu (34% vs 9%)
- Cần đánh giá lợi ích/nguy cơ khi phối hợp trên từng bệnh nhân cụ thể.
Kết luận lâm sàng
- Osimertinib đơn trị có hiệu quả hạn chế ở bệnh nhân UTPKTBN có di căn gan so với các vị trí di căn khác (não, xương).
- Các cơ chế vi mô và miễn dịch tại gan đóng vai trò then chốt trong hiện tượng đề kháng thuốc.
- Phối hợp với hóa trị có thể cải thiện đáng kể PFS, đặc biệt ở nhóm bệnh nhân mang đột biến exon19del hoặc có gánh nặng đột biến cao.
- Tương lai hướng đến phối hợp thêm thuốc ức chế tạo mạch (bevacizumab), chất ức chế MET hoặc liệu pháp miễn dịch chọn lọc.
Tài liệu tham khảo
- Clinical efficacy of osimertinib in EGFR-mutant non-small cell lung cancer patients with liver metastases. PubMed, 2022.
- Efficacy of EGFR-TKIs monotherapy versus TKI plus chemotherapy in advanced NSCLC with liver metastases. Front Pharmacol. 2021.
- NCCN Guidelines NSCLC v3.2025.
Cần tư vấn chuyên sâu về các thuốc điều trị ung thư phổi:
- ThS – BS Trần Khôi
- Bệnh viện Phổi Hà Nội – 44 Thanh Nhàn, Hai Bà Trưng
- Zalo: 0983 812 084 – Hotline: 0913 058 294
- Facebook: Bác sĩ Trần Khôi
- Kênh YouTube: Thạc sĩ Bác sĩ Trần Khôi – Chữa bệnh ung thư phổi




