XÉT NGHIỆM ĐỘT BIẾN EGFR, T790M TRONG MÁU DỰ BÁO HIỆU QUẢ OSIMERTINIB
23:22 - 25/09/2023
Osimertinib được khuyến cáo điều trị bước 2 sau khi kháng với thế hệ 1, 2 và có đột biến T790M(+).
Zongertinib là gì? Thuốc đích mới cho đột biến HER2 trong ung thư phổi
Hóa chất kết hợp kéo dài osimertinib hiệu quả tốt sau khi kháng osimertinib. Cập nhật nghiên cứu Compell 2025
Tiến bộ mới nhất 2025 trong điều trị ung thư phổi tế bào nhỏ (SCLC)
Hiệu quả của vắc xin CIMAvax trong điều trị ung thư phổi: Hy vọng mới cho bệnh nhân
NGHIÊN CỨU BIẾN ĐỔI ĐỘT BIẾN EGFR KHI ĐIỀU TRỊ OSIMERTINIB GIÚP DỰ BÁO HIỆU QUẢ OSIMERTINIB
Osimertinib, thuốc ức chế tyrosine kinase (TKI) EGFR thế hệ thứ ba, là tiêu chuẩn điều trị bước một đối với bệnh ung thư phổi không phải tế bào nhỏ giai đoạn muộn (NSCLC) có đột biến EGFR.
Đột biến EGFR T790M là cơ chế đề kháng ở khoảng 50–60% EGFR-TKI thế hệ 1, 2. Trong các nghiên cứu AURA và AURA2, osimertinib hiệu quả đáp ứng ở 61–70% khối u có T790M(+) kháng thuốc đích. Tuy nhiên, hiệu quả của osimertinib chỉ khoảng 10 tháng.
Sinh thiết mô được khuyến khích để xác nhận các bất thường về gen liên quan đến tình trạng kháng thuốc, nhưng có thể khó khăn do kích thước khối u nhỏ hoặc vị trí của các u nguyên phát hoặc di căn. Mặt khác, sinh thiết lỏng là một phương pháp đơn giản và nhẹ nhàng hơn.
Các nghiên cứu gần đây cho thấy rằng việc âm hóa các đột biến EGFR trong huyết tương sau khi bắt đầu điều trị EGFR-TKI bước 1 dự đoán đáp ứng với thuốc đích. Nghiên cứu này đánh giá sự biến đổi các đột biến EGFR(ex19del, L858R), T790M khi điều trị Osimertinib sau khi kháng thế hệ 1, 2 và giá trị dự báo hiệu quả Osimertinib.
1. Kết quả nghiên cứu
Đặc điểm bệnh nhân:
Từ 12/2016 đến 12/2019, 58 bệnh nhân có đột biến T790M(+) trong mô khối u hoặc huyết tương. Đặc điểm lâm sàng gồm:
- Độ tuổi trung bình là 68 tuổi (43–91)
- Đột biến EGFR ban đầu gồm exon 19del hoặc L858R. 01 bệnh nhân có đột biến T790M de novo cùng với L858R.
- 48 bệnh nhân (83%) có di căn giai đoạn lâm sàng IV khi chẩn đoán, 08 (14%) bệnh nhân tái phát sau phẫu thuật và 02 (3%) bệnh nhân tái phát sau hóa trị.
- 26 bệnh nhân (45%) có T790M(+) được xác nhận bằng sinh thiết lại mô, 06 (10%) tràn dịch màng phổi và 26 (45%) bằng sinh thiết lỏng.
Theo dõi đột biến EGFR huyết tương trong quá trình điều trị Osimertinib và khi bệnh tiến triển
Đánh giá tình trạng đột biến EGFR trong huyết tương được tiến hành sau mỗi 8 tuần điều trị với osimertinib.
Ban đầu, tỷ lệ đột biến kích hoạt EGFR và T790M là 81,0% và 75,9%. Tỷ lệ này giảm rõ rệt sau 8–16 tuần và tăng trong quá trình bệnh tiến triển (PD).
Trong 57 bệnh nhân, đột biến EGFR âm hóa ở 60,9% (28/46) và đột biến T790M âm hóa ở 93,0% (40/43). Trong đó, 71,4% (20/28) đột biến kích hoạt và 87,5% (35/40) đột biến T790M đã âm hóa trong vòng 8 tuần sau khi bắt đầu điều trị bằng osimertinib.
49 bệnh nhân tiến triển trong quá trình điều trị bằng osimertinib. Đột biến EGFR được phân tích ở 37/49 bệnh nhân, trong đó, đột biến EGFR(+) phát hiện ở 30 (81,1%) và T790M chỉ ở 13 (35,1%).
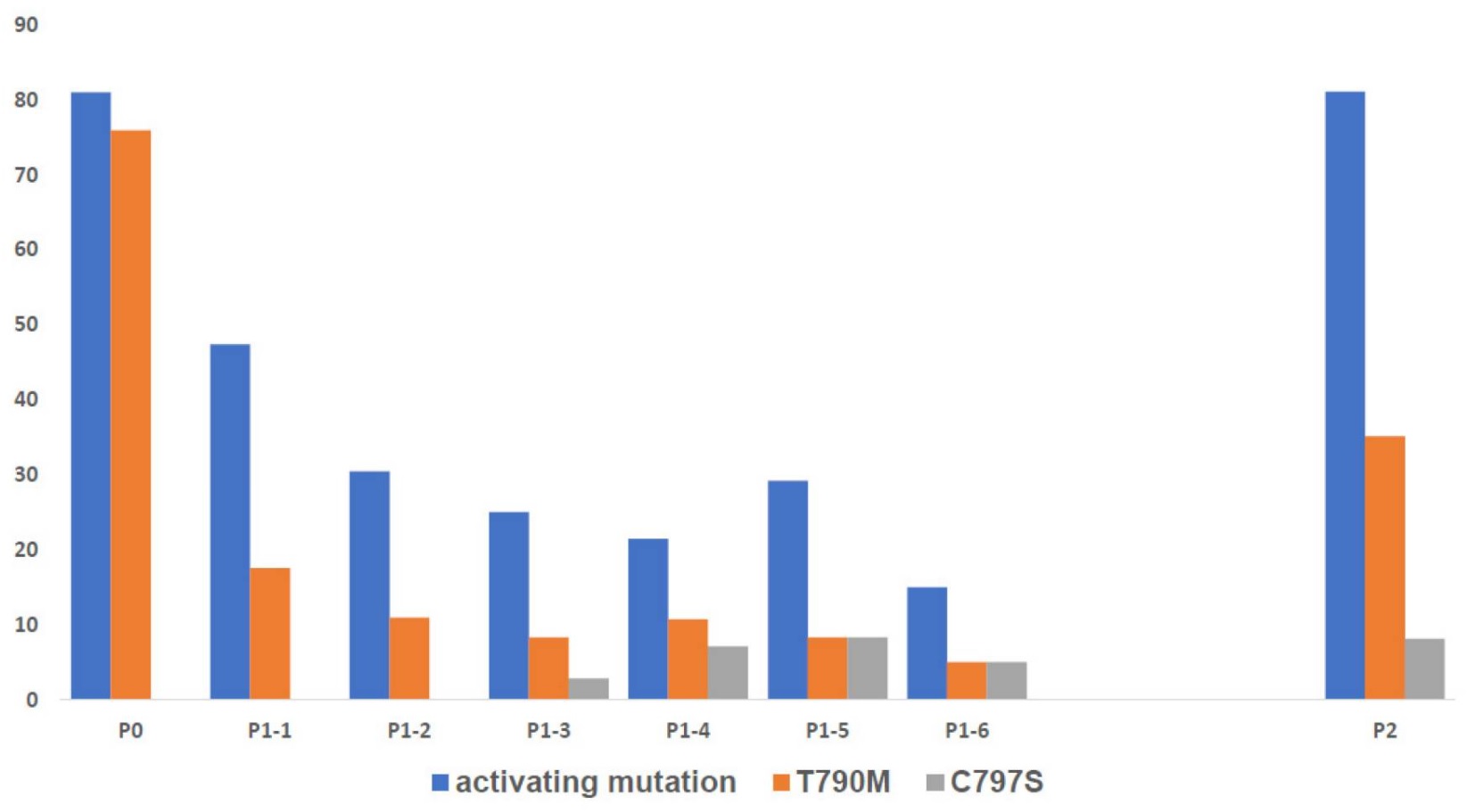
Đột biến EGFR và đột biến kháng thuốc T790M, C797S khi điều trị Osimertinib
P0: trước Osimertinib, P1-…: mỗi 8 tuần sau Osimertinib, P2: bệnh tiến triển
Hiệu quả của Osimertinib liên quan với tình trạng đột biến EGFR trong huyết tương ở bệnh nhân có đột biến EGFR T790M
01 bệnh nhân đạt đáp ứng hoàn toàn (CR), 30 bệnh nhân đáp ứng một phần (PR) và 23 bệnh nhân có bệnh ổn định (SD). Tỷ lệ đáp ứng khách quan (ORR) là 53,4%.
Khi so sánh đột biến EGFR trước khi điều trị Osimertinib (P0), EGFR âm tính có tỷ lệ đáp ứng cao hơn so với EGFR dương tính (81,8% so với 46,8%). Không có sự khác biệt giữa (+) và (-) đối với T790M (54,5% vs 50,0%).
- TTD trung bình (thời gian đến khi ngừng điều trị) dài hơn ở EGFR(-) huyết tương ban đầu so với EGFR(+) (15,3 tháng so với 7,8 tháng, p = 0,087 ).
- Nhóm có EGFR âm hóa sau 8 tuần điều trị có TTD dài hơn đáng kể so với EGFR không âm hóa (15,2 tháng so với 4,5 tháng, p < 0,01 ).
- Không có sự khác biệt về TTD giữa các trường hợp có và không có T790M khi bệnh tiến triển (P2) (9,5 tháng so với 8,5 tháng, p = 0,377).
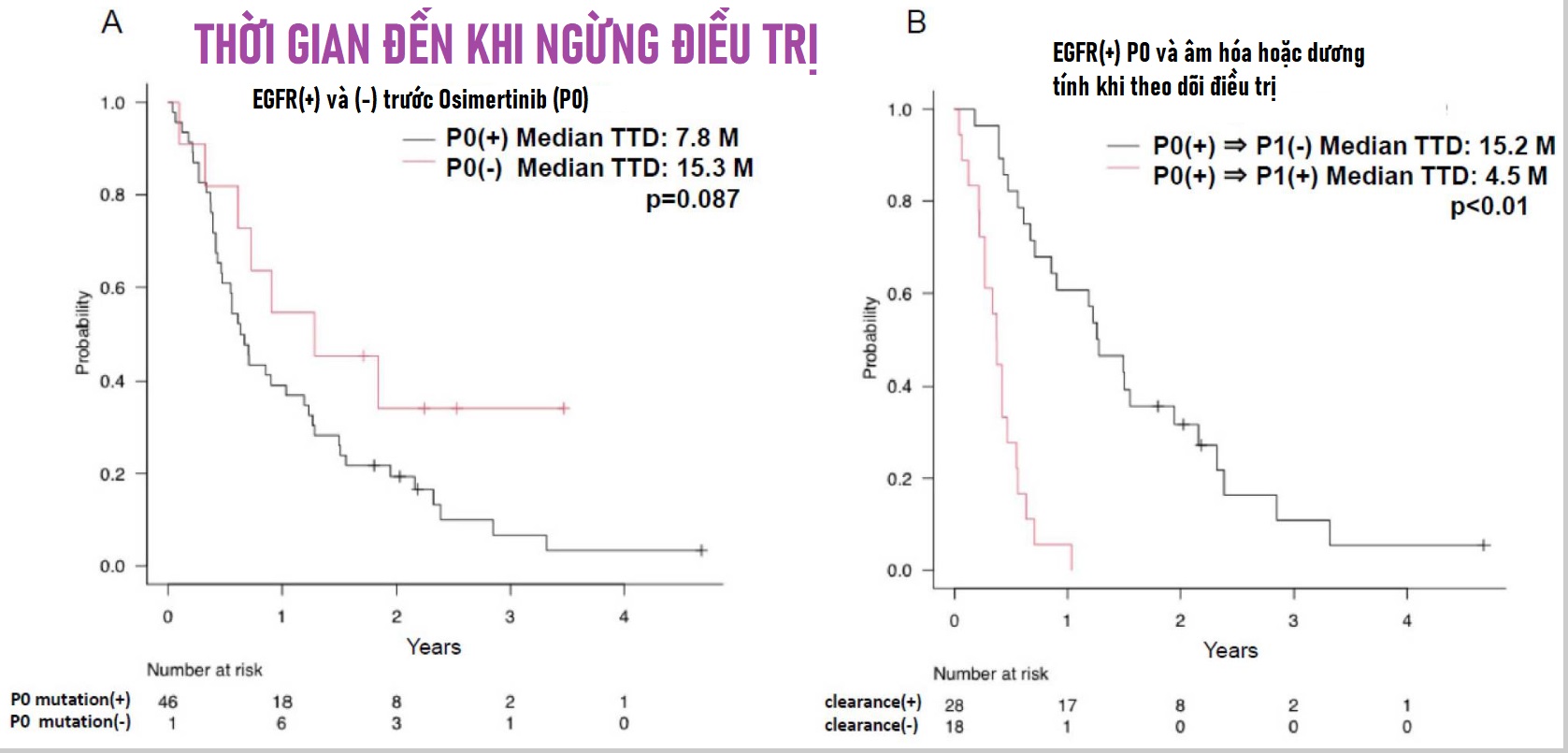
Đột biến EGFR(+) trước Osimertinib có TTD ngắn hơn EGFR(-)
Đột biến EGFR âm hóa khi điều trị có TTD dài hơn EGFR không âm hóa
2. Thảo luận
Nghiên cứu này nhằm mục đích nghiên cứu vai trò của việc theo dõi đột biến gen trong huyết tương khi điều trị osimertinib ở bệnh nhân tiến triển sau thuốc đích và dương tính với T790M.
Tần suất đột biến EGFR huyết tương trước điều trị (P0) là 81,0% và T790M là 75,9%. Đột biến EGFR(-) trước khi điều trị và âm hóa đột biến EGFR trong sinh thiết lỏng được chứng minh là có tính dự đoán về lợi ích điều trị.
Sử dụng phương pháp này, có thể thực hiện theo dõi huyết tương trong quá trình điều trị bằng osimertinib để dự đoán kết quả của điều trị.
Trong nghiên cứu này, TTD trung bình ngắn hơn đáng kể đối với nhóm có đột biến EGFR(+) ban đầu so với nhóm EGFR(-) và TTD trung bình dài hơn đáng kể đối với những bệnh nhân có đột biến EGFR âm hóa trong quá trình điều trị.
Trong thực hành lâm sàng, chẩn đoán bệnh tiến triển kháng thuốc dựa vào chẩn đoán hình ảnh. Tuy nhiên, theo dõi đột biến EGFR trong huyết tương xảy ra sớm hơn 6,0 tháng so với mức độ tiến triển trên chẩn đoán hình ảnh.
TÀI LIỆU THAM KHẢO
- Watanabe K, Saito R, Miyauchi E, Nagashima H, Nakamura A, Sugawara S, Tanaka N, Terasaki H, Fukuhara T, Maemondo M. Monitoring of Plasma EGFR Mutations during Osimertinib Treatment for NSCLC Patients with Acquired T790M Mutation. Cancers (Basel). 2023 Aug 24;15(17):4231. doi: 10.3390/cancers15174231. PMID: 37686506; PMCID: PMC10486675.




