THUỐC ĐÍCH LAZERTINIB MỚI SO SÁNH VỚI THẾ HỆ 1 GEFITINIB
08:16 - 25/04/2025
Thuốc đích thế hệ 3 mới Lazertinib so sánh với thế hệ 1 Gefitinib
Zongertinib là gì? Thuốc đích mới cho đột biến HER2 trong ung thư phổi
Hóa chất kết hợp kéo dài osimertinib hiệu quả tốt sau khi kháng osimertinib. Cập nhật nghiên cứu Compell 2025
Tiến bộ mới nhất 2025 trong điều trị ung thư phổi tế bào nhỏ (SCLC)
Hiệu quả của vắc xin CIMAvax trong điều trị ung thư phổi: Hy vọng mới cho bệnh nhân
Lazertinib So Với Gefitinib Trong Điều Trị Đầu Tiên NSCLC EGFR-Đột Biến: Phân Tích Kết Quả Từ Nghiên Cứu LASER301
1. Mở đầu
Ung thư phổi không tế bào nhỏ (NSCLC) là nguyên nhân hàng đầu gây tử vong do ung thư tại Hàn Quốc và trên toàn cầu. Sự phát hiện các đột biến hoạt hóa tại gen EGFR, đặc biệt là Exon 19 deletion (Ex19del) và L858R, đã làm thay đổi căn bản chiến lược điều trị. Trong số các nhóm bệnh nhân này, người châu Á (bao gồm Hàn Quốc, Nhật Bản, Việt Nam...) có tỷ lệ mang đột biến EGFR lên tới 30–60%, so với chỉ 10–30% ở người phương Tâycrt-2023-453.
Các thuốc ức chế tyrosine kinase EGFR (EGFR-TKI) thế hệ đầu đã chứng minh ưu thế hơn hóa trị về tỷ lệ đáp ứng và thời gian sống không bệnh (PFS). Tuy nhiên, hiện tượng kháng thuốc mắc phải, di căn não, và hiệu quả hạn chế trên đột biến L858R vẫn là rào cản lớn.
Để giải quyết vấn đề này, lazertinib – một EGFR-TKI thế hệ 3 – đã được phát triển và đưa vào nghiên cứu lâm sàng giai đoạn 3, nhằm so sánh với gefitinib – tiêu chuẩn điều trị hiện tại. Phân tích dưới đây dựa trên nhóm bệnh nhân người Hàn Quốc trong nghiên cứu toàn cầu LASER301.
2. Thiết kế nghiên cứu LASER301 – Phân tích nhóm bệnh nhân Hàn Quốc
2.1 Thiết kế & phương pháp
Thử nghiệm giai đoạn 3, ngẫu nhiên, mù đôi
So sánh lazertinib 240 mg/ngày với gefitinib 250 mg/ngày
Phân tầng theo đột biến EGFR (Ex19del hoặc L858R)
Tiêu chí chính: PFS do nhà nghiên cứu đánh giá (theo RECIST 1.1)
Các tiêu chí phụ: ORR, DoR, DCR, OS, an toàn, và dược động học
2.2 Đối tượng nghiên cứu
172 bệnh nhân Hàn Quốc được ngẫu nhiên hóa (lazertinib: 87, gefitinib: 85)
100% là ung thư tuyến, 98% giai đoạn di căn
Một phần ba có di căn não tại thời điểm bắt đầu
Tỷ lệ đột biến Ex19del vs. L858R: tương đương nhau (~57% vs. ~43%)
3. Kết quả hiệu quả điều trị
3.1 PFS – thời gian sống không bệnh
Lazertinib: 20.8 tháng (95% CI: 16.7–26.1)
Gefitinib: 9.6 tháng (95% CI: 8.2–12.3)
HR: 0.41 (95% CI: 0.28–0.60); p < 0.001
‼️ Lazertinib giúp giảm đến 59% nguy cơ tiến triển bệnh hoặc tử vong so với gefitinib.
Tỷ lệ không tiến triển sau 24 tháng:
Lazertinib: 45.0%
Gefitinib: 12.9%
3.2 Đáp ứng điều trị (ORR, DCR)
ORR: tương đương (~80% cho cả hai nhóm)
Nhưng DoR – thời gian duy trì đáp ứng:
Lazertinib: 19.6 tháng
Gefitinib: 9.0 tháng
=> Phản ứng kéo dài gấp đôi với lazertinib, cho thấy tiềm năng duy trì kiểm soát bệnh dài hạn.
4. Hiệu quả trên các nhóm đặc biệt
4.1 Bệnh nhân có di căn não
HR tiến triển hoặc tử vong: 0.28 (95% CI: 0.15–0.53); p < 0.001
PFS trung vị:
Lazertinib: 26.1 tháng
Gefitinib: 9.4 tháng
=> Khả năng xâm nhập CNS của lazertinib vượt trội rõ rệt. Đây là điểm then chốt vì 38–40% bệnh nhân EGFR+ có di căn não tại chẩn đoán.
4.2 Phân nhóm đột biến EGFR
Ex19del: HR = 0.43 (95% CI: 0.26–0.72)
L858R: HR = 0.36 (95% CI: 0.20–0.63)
=> Điểm đáng chú ý: Lazertinib có hiệu quả tốt cả trên đột biến L858R, vốn thường đáp ứng kém hơn các TKI trước đây.
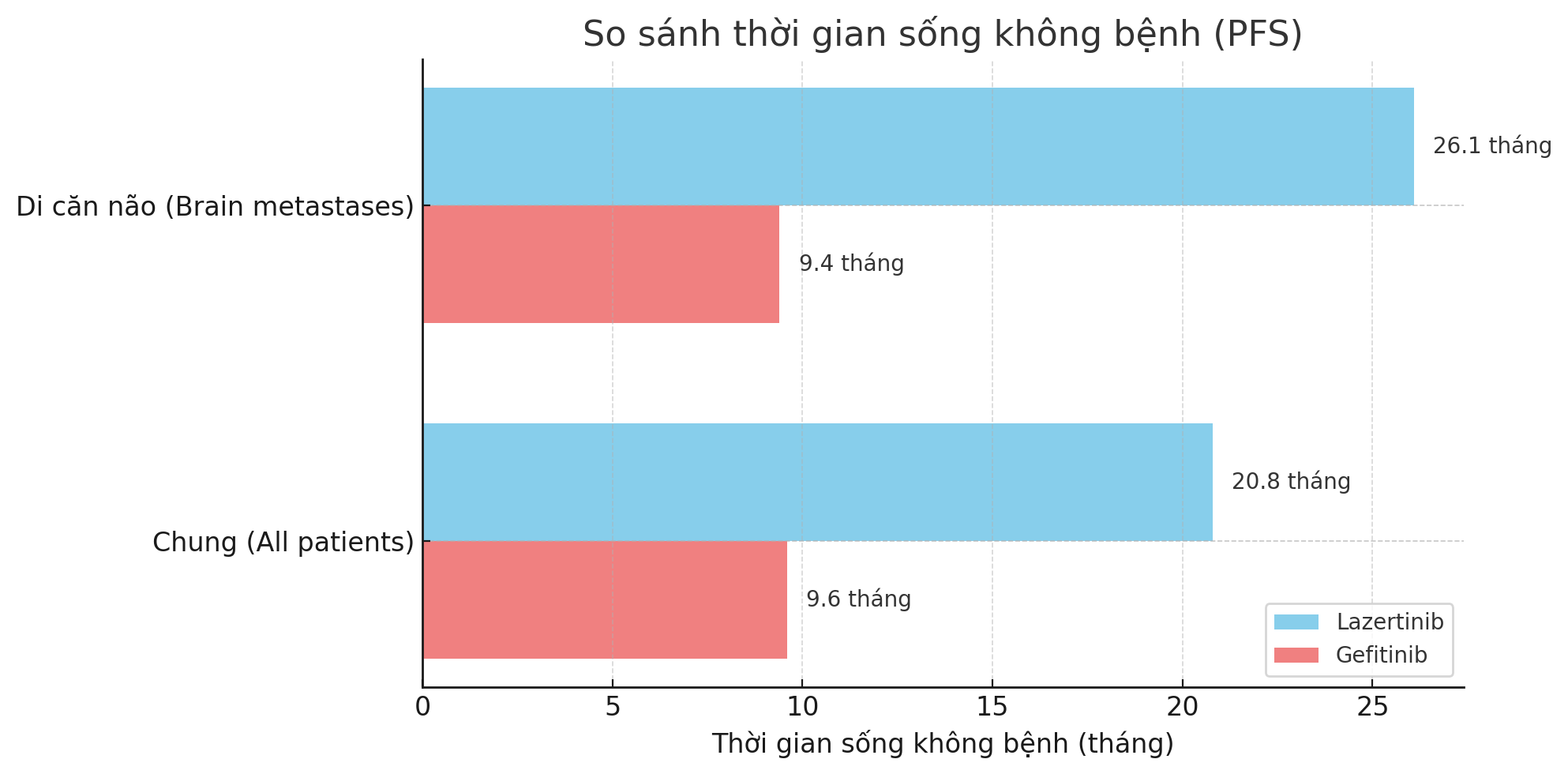
Hiệu quả vượt trội của Lazertinib kéo dài thời gian sống không tiến triển bệnh
5. An toàn và dung nạp
| Tác dụng phụ thường gặp | Lazertinib (%) | Gefitinib (%) |
|---|---|---|
| Paresthesia (dị cảm) | 52.9 | 8.2 |
| Phát ban | 46.0 | 50.6 |
| Ngứa | 43.7 | 35.3 |
| Tiêu chảy | 28.7 | 48.2 |
| Tăng men gan (ALT ≥ 3) | 1.1 | 10.6 |
Tác dụng phụ độ 3 trở lên: Lazertinib: 39.1% vs. Gefitinib: 50.6%
Không ghi nhận kéo dài QTc độ nặng ở nhóm dùng lazertinib
=> Lazertinib có hồ sơ an toàn tốt hơn, đặc biệt về tiêu hóa, gan và tim mạch.
6. Thảo luận: Tại sao Lazertinib là lựa chọn ưu việt?
6.1 Hiệu quả vượt trội so với thế hệ 1
Dữ liệu LASER301 xác lập lazertinib như lựa chọn đầu tay có hiệu quả PFS vượt trội so với TKI thế hệ 1.
Hiệu quả này duy trì ở cả các phân nhóm khó như: di căn não, L858R.
6.2 So sánh với osimertinib
Trong nghiên cứu FLAURA (osimertinib), mPFS ở châu Á: 16.5–19.1 tháng
LASER301 (lazertinib): 20.8 tháng → tương đương hoặc cao hơn
Lazertinib cũng có tác dụng mạnh lên CNS và ít tương tác với MDR1/BCRP, giúp thấm não tốt hơn osimertinib trong một số mô hình.
6.3 An toàn & chất lượng sống
Hồ sơ tác dụng phụ thuận lợi
Ít gây viêm phổi, kéo dài QTc, rối loạn gan nặng
Được đánh giá là thuốc chọn lọc mạnh với EGFR đột biến, tránh ảnh hưởng EGFR hoang dã
7. Hạn chế và hướng nghiên cứu tiếp theo
Dữ liệu OS còn chưa trưởng thành (28%), chưa thể kết luận về lợi ích sống toàn bộ
Có sự chuyển cánh (cross-over) từ gefitinib sang lazertinib sau tiến triển (~46%) → có thể làm lu mờ sự khác biệt OS
Chưa đánh giá cụ thể đáp ứng nội sọ (CNS-ORR), cơ chế kháng mắc phải – đang được tiếp tục nghiên cứu
8. Kết luận
Nghiên cứu LASER301 – phân tích nhóm bệnh nhân Hàn Quốc – khẳng định rằng lazertinib là một EGFR-TKI thế hệ 3 đầy triển vọng:
PFS vượt trội (20.8 vs. 9.6 tháng)
Hiệu quả ổn định ở bệnh nhân có di căn não
Duy trì đáp ứng kéo dài
Tác dụng phụ thấp hơn, dễ dung nạp
Hiệu quả cao trên cả Ex19del và L858R
=> Với hồ sơ dược lý vững chắc, lazertinib có tiềm năng trở thành chuẩn mới trong điều trị đầu tay NSCLC EGFR đột biến, đặc biệt ở bệnh nhân châu Á.
Tài liệu tham khảo chính:
Cancer Research and Treatment, 2024; 56(1):48-60.
NCT04248829 – LASER301 Trial
Cần tư vấn chuyên sâu về các thuốc điều trị ung thư phổi:
- ThS – BS Trần Khôi
- Bệnh viện Phổi Hà Nội – 44 Thanh Nhàn, Hai Bà Trưng
- Zalo: 0983 812 084 – Hotline: 0913 058 294
- Facebook: Bác sĩ Trần Khôi
- Kênh YouTube: Thạc sĩ Bác sĩ Trần Khôi – Chữa bệnh ung thư phổi




